Autor: Tomás Redondo. Catedrático de Biología. Educación Secundaria
01/06/2021
1. Actividad biológica del COVID 19.
El coronavirus es un virus que pertenece al grupo IV de la clasificación de Baltimore, lo que significa que es un virus con ARN I +. La I nos indica que la molécula de ARN es de una sola cadena y el signo +, que el ARN que transportan los viriones es el que lleva la información directa para la síntesis de las proteínas víricas1.
1 Los virus ARN I- se diferencian que la molécula que transporta el virión no codifica para sus proteínas. Debe sintetizarse otra molécula complementaria, que se usará para la formación de las proteínas del virus.
Una vez dentro del organismo, para penetrar en las células debe haber un reconocimiento entre proteínas de la membrana celular humana y proteínas de la envoltura del virus. En este cometido, tiene un papel muy importante la llamada proteína espiga del virus. Tras este reconocimiento, la envoltura del virus se funde con la membrana plasmática de la célula como dos pompas de agua y el virus queda libre en el citoplasma. Proteínas de la nucleocápsida vírica “se apropian” de la maquinaria biosintética de la célula y la ponen a disposición del virus.
Además de proteínas reguladoras y enzimas específicos del virus, se sintetiza una ARN polimerasa, dependiente de ARN, que cataliza la formación de moléculas de ARN vírico negativas (ARN-) Estas moléculas actuarán como plantilla para la fabricación de numerosas copias de ARN + . Una parte de estas estará destinada a la formación de los nuevos viriones (reproducción) mientras que la otra parte servirá para sintetizar las proteínas víricas, tanto funcionales como estructurales, que llevan los nuevos viriones.
Cuando todos los componentes del virus están sintetizados (ARN y proteínas de la nucleocápsida) se pasa a la fase de ensamblaje, en el aparato de Golgi y finalmente a la de expulsión de los nuevos viriones al exterior, proceso que tiene lugar por exocitosis. Durante todo el proceso, parte de las proteínas víricas pasan a la membrana de La célula infectada, donde pueden ser detectadas por el sistema inmune.
Los nuevos viriones que salen de las células pueden, bien infectar a otras o bien salir a las mucosas respiratorias o digestivas y de ahí transmitirse a otros individuos.
2. El sistema inmune frente al covid.
Al cabo de uno o dos días de la infección por el virus, en los fluidos corporales aparecen viriones libres y fragmentos moleculares del virus; también pueden aparecer estas moléculas en la superficie de las células infectadas. El sistema inmune interpreta como elementos extraños a todo lo expuesto anteriormente.
Estos elementos extraños inducen en el sistema inmune dos respuestas:
- Respuesta Inespecífica.- mediada por los fagocitos (principalmente macrófagos) y por las células NK2.
- Respuesta específica.- En sus dos vertientes humoral y celular. La primera la protagonizan los anticuerpos y la segunda diversos tipos de linfocitos T.
2 Células Natural killer, son células que matan a cualquier célula que presente sobre su MHCI moléculas ajenas al organismo.
Todas estas respuestas son complementarias y casi simultáneas. La vacunación frente a esta enfermedad pretende prevenir la infección por covid, estimulando al sistema inmune, para que produzca anticuerpos y células de memoria, para prevenir más adelante posibles infecciones. Hay que tener en cuenta, que en personas vacunadas, estas infecciones podrían producirse, pero al estar preparado el sistema inmune, reaccionaría rápidamente, de manera que la infección decaería enseguida.
El virus SARS-CoV-2 presenta en su envoltura varias clases de proteína. Una de ellas es la citada proteína espiga que emplea el virus para entrar en las células. Esta proteína, que es en realidad un trímero, ha sido elegida como proteína antigénica para la síntesis de las vacunas por todos los laboratorios, excepto por la marca sinovac.
3. Los diferentes tipos de vacunas contra el COVID
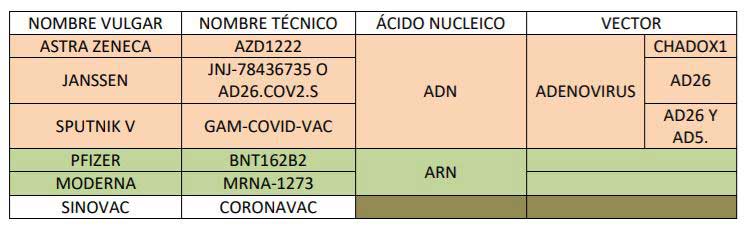
Cuando se escribe esto, a 1 de junio de 2021, Hay tres estrategias básicas en el diseño de vacunas frente al COVID. Dos basados en la tecnología de los ácidos nucleicos y una tercera con un diseño más clásico.
Las dos primeras familias de vacunas inducen a las células del individuo a sintetizar la proteína espiga; proceso que requiere dotar a la célula de la información genética necesaria para codificar su síntesis. ¿Cómo se introduce la información genética de espiga en las células del individuo? Se han seguido dos estrategias:
- Astra Zeneca , Janssen y Sputnik V, emplean como vector un virus artificial, en el que se introduce el gen que codifica para espiga. Los virus empleados por los tres laboratorios son distintas clases de adenovirus.
- Pfizer y Moderna introducen, no una molécula de ADN, sino de ARN y en este caso, emplean como vector nanopartículas lipídicas.
- Finalmente, la vacuna china sinovac ha optado por la elaboración de una vacuna clásica a base de virus desactivados, para que no puedan reproducirse.
4. Las vacunas de AstraZeneca, Janssen y Sputnik V
Esta Los adenovirus naturales son virus ADN II (bicatenarios) que pertenecen al grupo I de la clasificación del Baltimore, provocan resfriados con síntomas leves. Estos virus carecen de la capacidad de replicarse en células humanas.
Las vacunas AstraZeneca, Janssen y Sputnik V son más resistente al manejo que las vacunas de ARNm de Pfizer y Moderna por dos motivos: en primer lugar, las moléculas de ADN II son mucho más resistentes que las de ARN I; y en segundo, el gen de la proteína espiga está protegido por la envoltura del propio adenovirus; por estas razones, las vacunas de este tipo no tienen que permanecer ultracongeladas.
4.1. Mecanismo de acción
Después de inyectar la vacuna, los adenovirus se unen a las proteínas de la membrana celular, La célula la incorpora estos virus mediante endocitosis, con lo que el virus queda en el citoplasma envuelto en una vesícula. A continuación, el adenovirus sale de la vesícula y se introduce en el núcleo, donde se descapsida. El adenovirus no se puede replicar, pero si se puede transcribir. Las moléculas de ARNm resultantes de la transcripción saldrán al citoplasma, donde serán traducidas por los ribosomas.
Los ribosomas forman las subunidades proteicas que constituirán la proteína espiga; algunas de estas subunidades formarán espigas completas, mientras que otras permanecerán libres en el citosol.
4.2. Activación del sistema inmune
Tanto las subunidades de la espiga, como las moléculas espiga completas pueden emigrar hasta la membrana plasmática y unirse a las proteínas del MHC I3, que las exhibirá en la superficie celular.
Las células NK detectan a las células infectadas por el adenovirus y directamente las matan, aunque este efecto no es inmediato. Otro tanto hacen los linfocitos T, pero estos son aún más tardíos. La destrucción de estas células conlleva el derramamiento de su contenido y la aparición de moléculas de espiga (completas o incompletas) en el medio intersticial.
Muchas de estas moléculas son fagocitadas por los macrófagos, quienes las digieren parcialmente y trasladan los fragmentos moleculares resultantes a su superficie, donde se unen a las moléculas del MHCII4 . De esta forma, los macrófagos se convierten en células presentadoras de antígeno, recorrerán el sistema circulatorio, los órganos linfoides y los tejidos hasta dar con los linfocitos específicos. Los linfocitos Th reconocen estos fragmentos y liberan interleucinas (2, 4, 5 y 6 ) que estimulan a los linfocitos B, a los fagocitos y a los linfocitos Tc, cuya importancia veremos más adelante, al tratar de la supresión de las células infectadas.
3 Complejo principal de histocompatibilidad de tipo I; propio de todas las células nucleadas del organismo (los eritrocitos, no tendrían este complejo)
4 Complejo principal de histocompatibilidad tipo II. Presente en las células del sistema inmune.
Los AC son sintetizados por los linfocitos B tras ser estimulados por las proteínas espiga libres o presentadas sobre los MHC de los macrófagos. Esta activación solo afecta a aquellos linfocitos B que sean capaces de producir AC específicos y complementarios con la proteína espiga. Su activación consiste básicamente en formar un clon de células con dos destinos fundamentales: sintetizar AC y permanecer en “la reserva” en forma de células de memoria.
Los AC se unirán a las proteínas espiga, sea cual sea su origen: o pertenecientes a COVID que hayan infectado al individuo o adheridas a las células infectadas por el adenovirus. En el primer caso, los AC impiden la función de la proteína del COVID y este queda neutralizado; más tarde los macrófagos se encargarán de fagocitarlo. En el segundo caso, la presencia de AC en la superficie celular, supone un marcaje de la propia célula infectada, lo que significa que otros elementos del sistema inmune la considerarán una célula enferma que hay que eliminar. Así las cosas, cuando las células infectadas por el adenovirus de la vacuna -o por el coronavirus- presentan las proteínas de espiga en sus membranas plasmáticas, tanto los linfocitos Tc (células asesinas específicas) como las células NK procederán a su eliminación.
Los primeros AC que se sintetizan son del tipo IgM, formados por cinco unidades de Ig, al cabo de una semana empiezan a ser substituídos por los del tipo IgG, que permanecerán en circulación a lo largo de varios meses. La duración de la inmunización no se conoce con exactitud, aunque siempre hay que tener presente las células de memoria que se formaron durante la vacunación o durante la infección por COVID, en estas células encontramos tanto linfocitos B, como linfocitos T. La actividad de estas células puede extenderse a lo largo de varios años o incluso toda la vida. En este caso, hasta que no pase el tiempo suficiente, no podremos saberlo.
5. Vacunas de Pfizer-BioNTech y de Moderna
Estas vacunas se basan, como las anteriores en provocar la síntesis del antígeno espiga por las células del organismo, para estimular al sistema inmune. La diferencia estriba en dos aspectos:
- Las instrucciones para la síntesis de la proteína espiga se dan como una molécula de ARN (y no en forma de ADN, como pasaba con las anteriores).
- El vector empleado es una especie de nanoesfera lipídica y no un adenovirus, como lo que acabamos de ver.
Al ser la molécula de ARN muy frágil, hay que conservar la vacuna a temperaturas muy bajas (unos -70ºC Pfizer o -20ºC Moderna ).
5.1. Mecanismo de acción
Tras la inyección, las partículas de la vacuna se fusionan con las células y liberan el ARNm. Los ribosomas traducen la secuencia y sintetizan las proteínas espiga Este ARN, como cualquier ARN celular es destruido por los enzimas celulares y en no mucho tiempo desaparece. A partir
de aquí, los destinos de las proteínas espiga sintetizadas y la activación del sistema inmune son exactamente los mismos que los comentados para las vacunas de adenovirus.
6. Vacuna Sinovac
A diferencia de las anteriores, esta está basada en los propios virus COVID, desactivados. Esta vacuna tiene un diseño clásico, semejante al seguido en vacunas como la de la polio. La desactivación se consigue mediante el tratamiento de virus crecidos en células de riñón de mono con β-propiolactona. Esta sustancia desactiva la capacidad replicativa del virus, pero no altera las proteínas de su superficie (incluida la proteína espiga) Los virus así tratados, se unen a un adyuvante (compuesto de Al) que potencia la respuesta inmune.
6.1. Mecanismo de acción
Tras la inyección, los virus son interiorizados por células presentadoras de AG, que digieren las partículas y posteriormente, exhiben sus restos en la superficie celular, unidos a los complejos MHCII. A partir de aquí, los linfocitos Th y demás células del sistema inmune serán estimuladas contra los antígenos de la vacuna.
Del mismo modo que en los casos anteriores, los linfocitos B y T proliferarán, producirán anticuerpos, eliminarán las células que habían fagocitado los virus y además, unos y otros formarán células de memoria.